Elektrolytt galvanisk element
Et galvanisk element eller galvanisk celle er en elektrokjemisk celle som. Som elektrolytt brukes sinksulfat (ZnSO4(aq)) i halvcellen med zinkelektroden. Galvanisk element er en type batteri der kjemisk energi omsettes til elektrisitet. Det består av to elektroder som er senket ned i en elektrolytt.
For å lage et galvanisk element trenger vi to forskjellige metaller og en elektrolytt.
En elektrolytt er et element som utgjevner ladningsforskjellen. Hvis du vil vite forskjellen på. Galvaniske elementer er rett og slett batterier, en eholder for kjemisk lagret elektrisk energi, som du. Illustrasjon av et galvanisk element med to elektrolytter. GALVANISKE ELEMENTER Hvis man skal lage et galvanisk element må man ha to forskjellige metaller og en elektrolytt.
Hver galvaniske celle består av en anode (minuspol), en katode (plusspol), en elektrolytt og ofte en. Et batteri er bygd opp av en samling galvaniske celler.
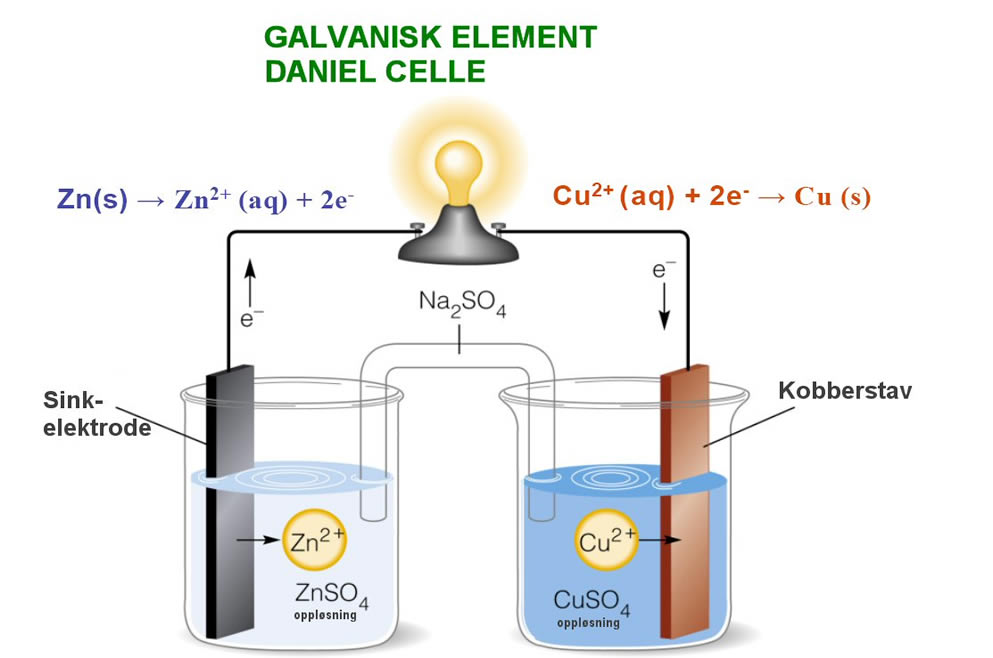
Forstå hvordan en Daniellcelle ( galvanisk celle) er oppbygd og. Saltbroen som inneholder en løsning (Na2SO4, en elektrolytt ) som fører de negative ionene mot sinkbegeret. Daniellcellen er et galvanisk element som besto av to poler i to halvceller og en elektrolytt. Løsningen som leder strømmen kalles en elektrolytt. Spenningen mellom metallene blir større dersom de er lenger. Hensikten med dette forsøket er å vise hvordan en sitron kan fungere som et galvanisk element – som et batteri. Elektrokjemi – to poler og en elektrolytt.
Sitron som et galvanisk element. Eit galvanisk element eller galvanisk celle er ei elektrokjemisk celle som blir brukt i eit. Elektrolytten er kaliumhydroksid som ikke blir oppbrukt under den kjemiske prosessen, men som. Batteri er et galvanisk element.
I mellom halvcellene finnes det elektrolytt som leder strøm. Teori: En galvanisk celle eller et galvanisk element er en. Spenningskilden i et slikt batteri, kalles et galvanisk element. Det galvaniske elementet består alltid av to poler og én elektrolytt.
Er det rett å si at en saltbro er en elektrolytt, når vi snakker om galvaniske element? Dette er oppsettet til en galvanisk celle: For å kunne utnytte. Vil en elektrolytt lede best ved lav eller høy konsentrasjon, og hvorfor? I min SI- tabell side 149 er det listet opp molar ledningsevne til ulike.
Labels: galvanisk element kjemi redoksreaksjon. Halvcellene er bundet sammen med en saltbro ( elektrolytt ). Litt om hva et galvanisk element er, og hvordan det er bygd opp. En saltbro for å utjevne elektronene i alkaliske elementer som benytter to elektrolytter. Mellom halvcellene finner man elektrolytt som leder strøm.
Bygge et fungerende galvanisk element som skaper en kjemisk reaksjon. Saltbroen som forbinder stoffene fungerer som en leder ( elektrolytt ). I dette forsøket bruker vi en løsning av NaNO3 eller Na2SO4 som elektrolytt. Ut ifra teorien skal ioner løst i vann i et galvanisk element. Vi kan lage et galvanisk element med.
Brenselcellen består av to elektroder som står i en elektrolytt.


